Pesquisadores sintetizam fármaco para tratamento de asma e fibrose pulmonar
Nova molécula protege contra inflamação neutrofílica e melhora função dos pulmões

Uma nova alternativa terapêutica para tratamento e controle de doenças respiratórias crônicas, como asma e fibrose pulmonar, é objeto de artigo publicado nesta semana na revista cientifica Nature Communications. Com um design molecular inovador, o CL27c foi projetado para terapia local – inalação pelas vias aéreas – de modo a reduzir os efeitos colaterais (toxicidade sistêmica) observados no uso do leque terapêutico atualmente disponível.
Desenvolvida pela spin-off Kither Biotech, na Universidade de Torino (Itália), e estudada no Laboratório de Imunologia e Mecânica Pulmonar do Instituto de Ciências Biológicas (ICB) da UFMG, a molécula CL27c foi criada com base em uma droga testada para tratamento de câncer. Contudo, a administração dessa classe de drogas a longo prazo acarreta efeitos colaterais como desenvolvimento do diabetes do tipo 2, com resistência a insulina e hiperglicemia persistente, arritmia cardíaca, imunossupressão e distúrbios intestinais, reduzindo a absorção de nutrientes.
O CL27c, por sua vez, tem a função de bloquear a atuação de umas das principais vias de comunicação intracelular, a PI3K, que também está diretamente ligada a processos de inflamação pulmonar e cicatrização tecidual – efeitos sintomáticos da asma e da fibrose pulmonar. O novo fármaco traz como novidade a mitigação desses efeitos indesejados, conforme explica o professor Remo Russo, do Departamento de Fisiologia e Biofísica. “Tal resultado foi possível devido à atuação específica e local da droga apenas nas vias aéreas, não atingindo níveis sistêmicos”, informa.
Pró-droga
O CL27c foi desenvolvido como pró-droga, isto é, fármaco administrado em forma inativa, sendo ativado somente após a biotransformação pelo metabolismo celular do paciente. ”Nossas observações mostraram que o inalado pode minimizar os efeitos tóxicos da exposição sistêmica de inibidores de PI3K”, ressalta Remo Russo. Os resultados alcançados em modelos pré-clínicos de asma grave e fibrose pulmonar irreversível revelaram que a nova molécula “pode abrir um caminho para futuras aplicações clínicas”, diz o pesquisador.
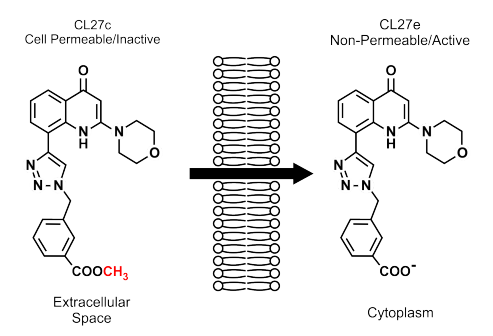
Nos testes com cobaias, os resultados in-vivo confirmaram que a atuação do fármaco ficou restrita apenas àquelas células respiratórias, bloqueando a ação da PI3K sem induzir a efeitos colaterais de resistência a insulina. Os animais manifestaram redução das atividades inflamatórias e fibrogênicas. Também foram constatados bons resultados em indivíduos com baixo índice de aceitação de tratamentos tradicionais, à base de anti-inflamatórios corticoides.
O novo fármaco apresentou atividade anti-inflamatória, por inibir células do sistema imune – como eosinófilos e linfócitos – relacionadas às respostas alérgicas clássicas, além de minimizar a produção de muco e a fibrose bronquial, característicos da asma, o que, em conjunto, melhora a função pulmonar. Segundo o professor, embora os corticosteróides sejam o tratamento de base para essas doenças, até 10% dos pacientes com asma grave apresentam resistência à corticoterapia.
A pesquisa também constatou que o CL27c inalado de maneira terapêutica protege da inflamação neutrofílica crônica e da indução de genes marcadores de atividade de fibroblastos, reduzindo da fibrose pulmonar e, em última instância, a uma melhora significativa da função pulmonar, com reflexo no aumento da sobrevida dos animais tratados. O estudo concluiu ainda que o CL27c administrado em cultura celular (in vitro) reduz a atividade de fibroblastos isolados de pacientes com Fibrose Pulmonar Idiopática (IPF, na sigla em inglês), o que sugere também um papel anti-fibrogênico dessa molécula.
Trabalho conjunto
Remo Russo explica que o artigo é fruto de pesquisas que tiveram como ponto de partida o seu doutorado. “Em 2011, publicamos um trabalho cuja conclusão mostrava que a via PI3K consistia em atuação direta no recrutamento de células inflamatórias e de fibrogênicas dos tecidos pulmonares, que provocam a fibrose pulmonar. Posteriormente, em trabalhos colaborativos, procuramos desenvolver uma molécula que fosse capaz de inibir a PI3K sem tais efeitos colaterais”, explica. Segundo ele, participaram do estudo, como colaboradores, pesquisadores da Universidade de Torino, da Faculdade de Medicina da Universidade de São Paulo (USP) de Ribeirão Preto e da Universidade Federal do Ceará (UFC).
Grande parte dos experimentos foi conduzida por Matheus Mattos e Lucas Kraemer, alunos do Programa de Pós-graduação em Fisiologia e Farmacologia da UFMG. O trabalho também contou com a participação de pesquisadores dos departamentos de Patologia e de Imunologia do ICB.
Doenças que matam
Segundo dados mais recentes da Pesquisa Nacional de Saúde (2013), do Instituto Brasileiro de Geografia e Estatística (IBGE), no Brasil, 6,4 milhões de pessoas com mais de 18 anos são acometidas pela asma. No país, é a doença crônica, ou seja, com progressão lenta e longa, mais comum. Incluindo crianças e idosos, o índice salta para aproximadamente 20 milhões. A doença se caracteriza por inflamações frequentes no sistema respiratório, acarretando a produção excessiva de muco e a dificuldade de respirar.
A fibrose pulmonar idiopática se caracteriza pela cicatrização excessiva do tecido, diminuindo progressivamente a sua capacidade respiratória e difusora. A enfermidade tem causa desconhecida e, apesar da evolução lenta e progressiva, costuma levar o paciente a óbito em até cinco anos após o seu diagnóstico. Como não há terapia eficaz, as únicas alternativas são o uso de paliativos e, em último caso, o transplante.